"La ciencia será siempre una búsqueda, jamás un descubrimiento real. Es un viaje, nunca una llegada"
Karl R. Popper
Claudia Elena
Arias Navarro
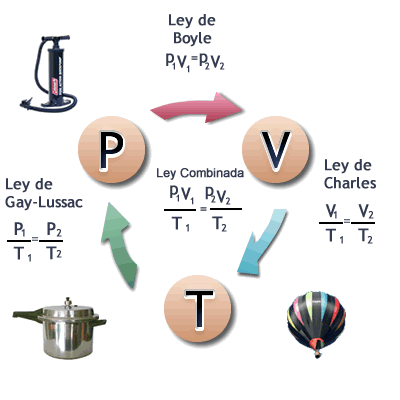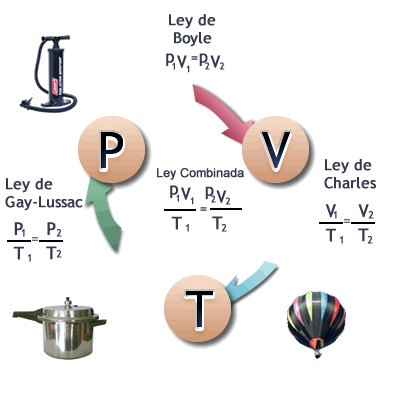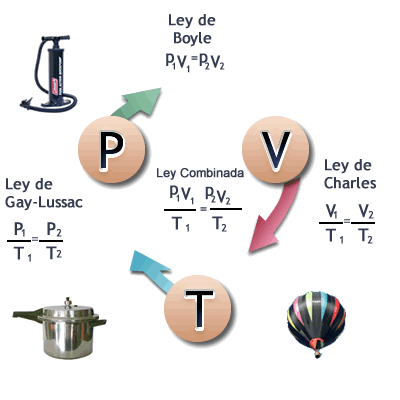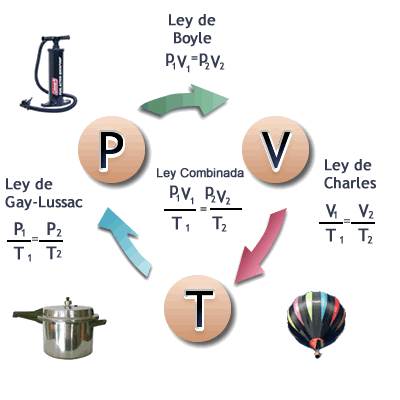
ejercicios propuestos
1. Responda las siguientes preguntas y justifique su respuesta de acuerdo a las leyes de los gases (Valor 1 punto)
1.1. La ley de Boyle establece que la presión y el volumen de un sistema gaseoso son inversamente proporcionales. Según esto, si aumentamos el volumen de un gas al doble, ¿qué le ocurre a la presión del mismo?
1.2. En el envase de cualquier aerosol podemos leer que no debemos arrojarlo al fuego ni aún vacío. ¿Por qué el fabricante está obligado a hacer esa advertencia? ¿En qué ley de los gases te basarías para explicar la advertencia?
2. Resuelva los siguientes ejercicios y enuncie la ley de los gases que usas para hacer el problema. (Valor 3 puntos)
2.1. Un gas ocupa un volumen de 250 mL a la temperatura de 293 K. ¿Cuál será el volumen que ocupe cuando su temperatura sea de 303 K?
2.2. Qué volumen ocuparán 500 mL de un gas a 600 torr de presión si se aumenta la presión hasta 750 torr a temperatura constante?
2.3. ¿Qué presión hay que aplicar a 2,0 L de un gas que se encuentra a una presión de 1,0 atm para comprimirlo hasta que ocupe 0,80 L?
2.4. En un recipiente se tienen 16,4 litros de un gas ideal a 47ºC y una presión de una atmósfera. Si el gas se expande hasta ocupar un volumen de 22 litros y la presión se mantiene constante ¿cuál será la temperatura final del sistema?
2.5. Si cierta masa de gas contenido en un recipiente rígido a la temperatura de 100ºC posee una presión de 2 atm, ¿qué presión alcanzará la misma cantidad de gas si la temperatura aumenta a 473 K?
2.6. Si el volumen resulta ser de 4 litros y la temperatura 20ºC, y calentamos el aire hasta 200ºC ¿cuál será el Volumen de aire (del recipiente)? ¿Y si lo enfriamos hasta 0ºC?
3. Determine qué ley de los gases se aplica en cada caso y explique (Valor 1 punto)
3.1. Al calentar un globo aerostático, el gas del globo tiende a expandirse más; es decir, su volumen aumenta, logrando elevar el globo a mayor altura.
3.2. En las ollas a presión, si calientas la olla, el gas en su interior aumenta su presión. (el volumen es constante)
3.3. a temperatura constante, SI elevamos la presión digamos subiendo a un cerro alto y contuviéramos la respiración en este proceso el aire (que es un gas) bajaría el volumen y contraería nuestros pulmones.